Anaerobní metanolový denitrátor
– princip a praktické zkušenosti s použitím v mořských akváriích
(spoluautorem článku je Miroslav Buršík)
Úvod
V tomto článku bych se chtěl podělit o zkušenost s řešením problému postupné akumulace dusičnanů v akváriu. Mořský svět na pražském Výstavišti, který je „místem činu“, vznikl v roce 2002. Propojení velké části akvárií na centrální filtraci proběhlo o pár let později. Jedná se tedy o starý systém, kde za dobu jeho fungování nastoupala koncentrace dusičnanů až k „neměřitelným“ hodnotám. Tento problém bylo třeba vyřešit. Ale jak se efektivně zbavit dusičnanů ve 20 000 l mořské vody, ideálně s co nejnižšími náklady?Takových akvarijních systémů pravděpodobně v České republice moc není. Nicméně věřím, že zkušenosti a principy zde popsané mohou být přínosné pro většinu akvaristů, a to jak pro ty s mořskými nádržemi, tak i sladkovodními.
Akumulace živin v akváriu
Každé krmení ryb či jiných obyvatel akvária obsahuje bílkoviny neboli proteiny. Ty jsou základním stavebním kamenem života, a tak jsou zcela nezbytné. Bílkoviny jsou tvořené aminokyselinami, které jsou z definice sloučeniny obsahující aminovou skupinu (NH2). Pokud organismus potřebuje z potravy syntetizovat bílkoviny např. pro svůj růst, využije je beze zbytku. Nicméně pokud potřebuje jen energii, dusík nevyužije a musí ho vyloučit. Tím nevyhnutelně přidáváme dusík do akvária při každém krmení.
Podobné je to i s fosforem, který je obsažen v těch nejdůležitějších sloučeninách – DNA, RNA nebo ATP.
Pokud bychom uvažovali uzavřený systém bez způsobu exportu těchto prvků, koncentrace dusíku a fosforu bude s krmením neustále postupně narůstat.
Koloběh dusíku
Koloběh dusíku je jedním z nejdůležitějších dějů, které v akváriu probíhají. Je to základ fungování uzavřeného ekosystému, který se snažíme vytvářet.
Ryby vylučují dusík v podobě toxického amoniaku. Ten se musí co nejrychleji přeměnit na jinou formu, která tak toxická není. To nám zajišťují nitrifikační bakterie, které přeměňují oxidací amoniak na dusitany a posléze na dusičnany. Při tomto procesu vzniká energie, kterou mohou využívat pro svůj metabolismus. Protože využívají oxidaci, musí tento proces probíhat v prostředí s dostatečnou koncentrací rozpuštěného kyslíku. Proto musí být ve filtru stále dostatečný průtok vody, abychom zajistili tzv. aerobní prostředí a bakterie si mohly spokojeně oxidovat.
Noční můra každého akvaristy je tzv. anaerobní zvrat – když se průtok zastaví nebo z jiného důvodu dojde k poklesu kyslíku, vytvoří se anaerobní prostředí a dusičnany se začnou přeměňovat zpět na amoniak. Pak může dojít k otravě a vymření akvária.
Dusitany a hlavně dusičnany jsou výrazně méně toxické než amoniak. Nicméně dlouhodobá zvýšená koncentrace dusičnanů může mít mnoho negativních dopadů na naše chovance.
Sladkovodní vs. mořská akvaristika
Zde se docela zásadně liší přístup k dusičnanům mezi sladkovodním a mořským akváriem. Následující dva odstavce ilustrují tento rozdíl, ale jedná se o velmi stručný nástin a zjednodušující pohled.
Sladkovodní – hlavní způsob omezování dusičnanů jsou výměny vody. Za bezpečnou se udává koncentrace mezi 50–100 mg/l. V případě zvířat žijících ve velmi čistém prostředí, např. rychle tekoucí říčky, se doporučuje výměna až 50 % vody za týden (ale pozor – v pitné vodě může být až 50 mg/l dusičnanů).
Mořská – nejčastěji doporučovaná koncentrace dusičnanů je maximálně 10 mg/l. Významné výměny vody nejsou žádoucí (do 10 % objemu). Proto je nutné buď výrazně limitovat množství krmení, nebo nějakým způsobem snižovat koncentraci dusičnanů.
Export dusičnanů
Jaké jsou možnosti, pokud chceme aktivně snižovat množství dusičnanů? Ve sladké vodě jsou to hlavně již zmíněné výměny vody a potom rostliny. Ty využívají dusík rozpuštěný ve vodě ke svému růstu.
I v mořském akváriu nám nejvíce pomáhá výměna vody. Sice na objem nemůže být tak výrazná, ale díky využití vody z reverzní osmózy neobsahuje vstupní voda žádný dusík. Autotrofních organismů máme na výběr více – obdobně jako rostliny ve sladké vodě fungují v mořských akváriích koráli a různé druhy řas nebo rostlin.
Mnoho akvaristů zařazuje do systému tzv. refugium – oddělení filtru určené k pěstování makrofyt, např. zelených řas z rodu Chaetomorpha nebo Caulerpa. Další možnost, jak využít řasy, je „Algae turf scrubber“ – v tomto filtru kape voda přes osvětlenou mřížku, kde narůstá mikro řasa v podobě „koberce“. Pravidelným odstraňováním biomasy řas dochází k odstraňování dusíku ze systému.
Pravděpodobně nejoblíbenější metodou je přidávání přípravků, které snižují obsah živin ve vodě. Jedná se např. o „NO3 : PO4 – X“ od Red Sea nebo Tropic Marin „ElimiNP“. Na podobném principu pracuje i reaktor na biopelety. Jaký je to princip?
Denitrifikace
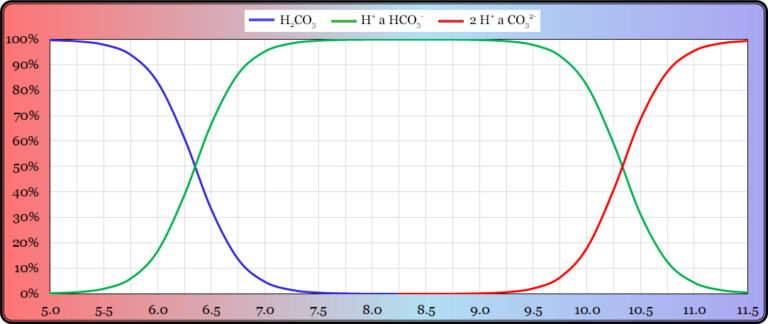
Nitrifikace je oxidace dusíkatých sloučenin za asistence bakterií z amoniaku přes dusitany na dusičnany. Reakce vypadají takto:
1. nitritace: NH3 + O2 –> NO2− + 3H+ + 2e−
2. nitratace: NO2− + H2O –> NO3− + 2H+ + 2e−
Denitrifikace je opačný proces – redukce dusičnanů až na molekulární dusík. Ten potom z vody vyprchá do atmosféry (kde je dusík nejčastější prvek). Zjednodušená reakce denitrifikace, kde A je substrát, který bakterie za pomoci NO3– redukuje:
Ared + NO3– –> Aox + N2 + energie
Oxidace probíhá v prostředí s vysokou koncentrací kyslíku, redukce tam, kde je kyslíku nedostatek.
Denitrifikace je velmi dobře popsaný proces, který se masivně využívá v čistírnách odpadních vod. Neprobíhá samovolně – je energeticky nevýhodná, takže redukující bakterie potřebují substrát. Základním způsobem, jakým živé organismy získávají energii, je přeměna složitějších uhlíkatých látek na jednodušší. To souhrnně nazýváme katabolismus. V našem těle je nejčastějším procesem přeměna glukózy až na oxid uhličitý. Pamatujete si ze školy rovnici C6H12O6 + 6 O2 + 6 H2O –> 6 CO2 + 12 H2O ?
Důležité pro nás je, že se jedná také o oxidaci, při té totiž vždy vzniká více energie. Bez kyslíku to jde taky – zapojí se tzv. anaerobní metabolismus, který občas též probíhá i v našich tkáních. Pokud naše svaly spálí výše uvedenou reakcí všechen kyslík, začnou přeměňovat glukózu na kyselinu mléčnou. Tato reakce není tolik výhodná, proto v anaerobním metabolismu nedokážeme fungovat příliš dlouho.
Co to má společného s denitrifikačními bakteriemi? I ony přeměňují složitější uhlovodíky na jednodušší a získávají tak energii. A i pro ně je výhodnější využít oxidace a získat z každé molekuly více energie. Jenomže pokud není kyslík obsažen ve vodě, pokud tyto bakterie žijí v anaerobním (nebo anoxickém) prostředí, jsou schopné využít kyslík z dusičnanů, které tak přemění na dusitany a ty na molekulární dusík.
Vrátím se tedy k fungování kouzelných vodiček – není to nic jiného než zdroj uhlíkatých látek, které využívají bakterie dvěma způsoby. V prostředí s dostatečnou koncentrací kyslíku jako zdroj snadné energie, což jim umožní rozmnožování a k růstu nových buněk využijí i nějaký ten dusík z vody (vytváří biomasu, která je odstraněná ve filtraci nebo odpěňovači). V prostředí bez dostatečné koncentrace kyslíku (např. v substrátu nebo uvnitř živých kamenů) pak hraje prim právě denitrifikace.
Denitrifikace v praxi
Nyní bych rád přistoupil k druhé části článku – případové studii využití denitrifikace v praxi.
Popis systému a výchozí stav
Systém, kterému se budeme věnovat, má celkový objem přibližně 20 000 l mořské vody. Je to 13 akvárií svedených do jednoho „sumpu“, kde probíhá filtrace a úprava vody. Akvária jsou výstavní nádrže zaměřené hlavně na ryby – žijí v nich např. murény, perutýni, žralůčci nebo chobotnice. Biologická zátěž je tak značná. Zároveň se v této zátěži nedařilo korálům a za cca. 15 let fungování nastoupala koncentrace dusičnanů až k hodnotám mezi 150–200 mg/l. Ruční kolorimetrické testy jsou v těchto koncentracích vysoce nepřesné, takže jsme využívali laboratoř Tritonu a jeho produkt N-DOC – stanovení přesné koncentrace dusíku a rozpuštěných uhlíkatých látek. Bohužel je tak možné stanovit jen celkový dusík rozpuštěný ve vodě a nikoliv jeho formu.
Dávkování uhlíku
První pokus o snížení koncentrace NO3– byl přidáváním uhlíkatého substrátu přímo do vody, tak jako je tomu v případě již zmiňovaných komerčních produktů. Výhod je mnoho – není zapotřebí žádné další zařízení; bakterie, které začnou růst, mohou využívat filtrátoři ke své obživě; a spekuluje se i o tom, že jsou koráli schopní přímo využívat organický uhlík z vody. Za zdroj uhlíku je nejlépe využít etanol, metanol nebo acetát. Metanol je jedovatý a není vhodné ho přidávat přímo do akvária. Etanol je zatížený vysokou spotřební daní, takže nejvýhodnější je využití kyseliny octové – octa. Je vhodné lít kyselinu do akvária, kde se snažíme udržovat zásadité pH min. 8,0? Kyselina octová je tak rychle využitá bakteriemi a přeměněná, že to s hodnotou pH vůbec nepohne.
Tato metoda fungovala poměrně účinně. Po 2 měsících postupného zvyšování dávek octa se denní dávka ustálila na 1,5 l 10% kyseliny octové. Za měsíc se snížila koncentrace rozpuštěného dusíku o cca. 20 %.
Jenomže produkovaná bakteriální biomasa byla absolutně nezvládnutelná – na všech površích v akváriích byli provazce a chuchvalce bakteriálního „slizu“. Jeden den po úklidu a odsátí byl nárůst zpět. V domácím akváriu bych to vydržel – zatnul zuby, často odkaloval a za 5 měsíců by byl problém dusičnanů vyřešený. Ale estetický dopad na naší expozici byl takový, že jsme nemohli touto metodou dále pokračovat.
Denitrátor
Volba tedy padla na vytvoření bioreaktoru, kde bude denitrifikace a růst bakterií probíhat v kontrolovaném prostředí a bez viditelného dopadu na estetickou kvalitu akvárií.
Takové reaktory jsou běžnou součástí čistíren odpadních vod, ale v akvaristice se využívají jen velmi zřídka. Akvaristé jsou od samých začátků s prvním akváriem naučení, že anaerobní podmínky jsou zlé a mohou způsobit velký problém. Proto si myslím, že je pro většinu chovatelů neintuitivní cíleně vytvořit filtr s anaerobním prostředím.
Jako uhlíkatý substrát pro krmení bakterií je zde nejvýhodnější použít metanol – jsou s ním nejlepší zkušenosti, navíc je poměrně levný i v laboratorní kvalitě.
Anaerobní procesy jsou méně efektivní než aerobní, probíhají tedy vždy pomaleji. To znamená, že v reaktoru musí být akvarijní voda dostatečně dlouho, aby bakterie stihly využít veškerý metanol ke kompletní denitrifikaci. Pomalý průtok je i nezbytný pro vytvoření anaerobních podmínek – nitrifikační bakterie musí využít v povrchové vrstvě reaktoru všechen kyslík.
Jaká jsou rizika takového zařízení?
- Nedokonalé odstranění metanolu – pokud voda proudí příliš rychle, tak nestihnou bakterie využít všechen metanol. Podobně pokud koncentrace dusičnanů a dusitanů klesne na nulu, reakce se zastaví. Navíc mohou bakterie začít využívat jiné látky, např. sloučeniny síry, a může tak vznikat toxický sulfan.
- Nekompletní denitrifikace – do vody se pak mohou dostat nežádoucí meziprodukty, hlavně dusitany.
- Technická závada – pokud dojde k poruše, nesmí se obsah reaktoru (s nezreagovaným metanolem a nebezpečnými sloučeninami dusíku) dostat zpět do systému.
- Ucpání bakteriální biomasou – pokud by se reaktor ucpal, hrozí nastoupání koncentrace metanolu a vymření bakteriální populace, která se pomalu obnovuje.
Takže, jaké byly designové požadavky na tento reaktor?
- Kontaktní doba (čas, po který je voda v reaktoru a může probíhat reakce): 4–6 hodin.
- Pokud možno co nejlepší rozdělení průtoku vody skrz celý reaktor.
- Dobré promíchání metanolu a vstupní vody.
Minimalizace rizik:
- Co největší průměr trubek a fitinek v samotném reaktoru – aby se minimalizovalo riziko ucpání bakteriální biomasou.
- Voda ze systému do reaktoru i z reaktoru zpět do systému proudí pouze přepadem, který je umístěný nad hladinou vody. Nehrozí tak odčerpání obsahu reaktoru sifonovým efektem zpět do systému při poruše.
- Hlídání průchodnosti reaktoru – pokud se začne ucpávat biomasou, je nutné okamžité vyčištění.
- Předřazení reaktoru před další filtraci, hlavně odpěňovač.
Technické provedení
Jako reakční nádobu jsme využili polypropylenový válec ze starého odpěňovače o průměru 47 cm, výšce 150 cm a objemu 260 l. Reaktorem voda stoupá a přepadem se dostává zpět do akvária. Přívodní trubka má průměr cca 10 cm a je ode dna reaktoru vyvedena vzhůru až nad hladinu. Tam je volně zakončená a padá do ní voda z čerpadla. To tlačí vodu ze systému průtokem cca 50 l/h (hlídáno průtokoměrem). Retenční doba v reaktoru je tedy přibližně 5 hodin.
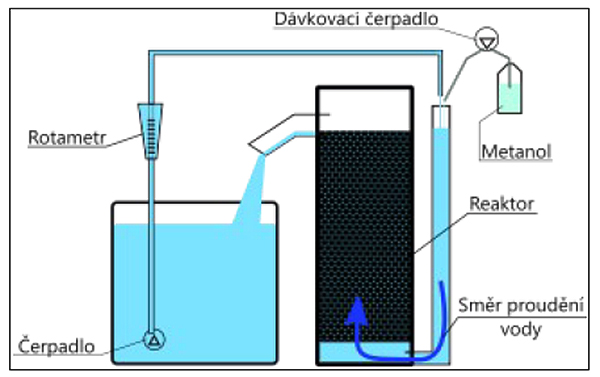
Na rozdílu hladin mezi reaktorem a přívodní trubkou je vidět průchodnost filtru. Na dně reaktoru je umístěn difuzor – deska s několika otvory v celém obsahu, která usměrňuje a rozděluje proud vody skrz celý průřez válce.

(Foto: Mikuláš Velenský & Miroslav Buršík)

(Foto: Mikuláš Velenský & Miroslav Buršík)
Jako biologické médium pro osídlení bakteriemi jsme zvolili plastové filtrační kuličky „bioballs“. Ačkoliv mají menší funkční plochu než jiná média, jejich výhodou pro toto použití jsou poměrně velké mezery, takže se hůře ucpávají. Pokud je nárůst biomasy značný, dají se snadno vyprat.
Metanol je dávkovaný do přívodní vody dávkovacím peristaltickým čerpadlem. Dávkujeme 50% zředěný metanol s osmotickou vodou jedenkrát za dvě hodiny (12x za den).

(Foto: Mikuláš Velenský & Miroslav Buršík)
Měření
Měření dusičnanů ve vstupní a výstupní vodě je pro úspěch denitrifikátoru kritické. Dusičnany se měří poměrně těžko, ruční kolorimetrické testy nemají dostatečnou přesnost a jejich interpretace není snadná. Vysoké hodnoty, které byly v systému původně, jsme tedy přesně změřili jen laboratorním testem N-DOC od firmy Triton. Ale protože je nutné vzorek vody odeslat do Německa, trvá přibližně týden, než přijdou výsledky. Proto jsme v průběhu zabíhání pořídili ruční elektronický kolorimetr Hanna Checker Nitrates LR. S ním jsme schopní dosáhnout konzistentních výsledků s přesností na desetinu mg/l.
Záběh
Zabíhání anaerobního filtru trvá dlouho – anaerobní metabolismus je pomalejší a bakterie se pomaleji množí. Naplánovali jsme období dvou měsíců s postupným zvyšováním dávky metanolu. V tomto období jsme měřili každý den koncentraci dusičnanů v systému a ve výstupu z reaktoru a dávku metanolu upravovali dle výsledků. Maximální efektivity dosáhl reaktor po 105 dnech, kdy je vidět prudký propad koncentrace dusičnanů.
Výsledky
Výsledky jsou pro mě vpravdě ohromující. Za tři měsíce jsme vyřešili problém, o kterém jsem si myslel, že se potáhne roky. Na cílovou hranici kolem 10 mg/l jsme se dostali po 119 dnech (12,8 mg/l). K redukci dusičnanů na tuto hranici spotřeboval denitrátor cca 14 l metanolu, což je v nákladech neuvěřitelně nízkých 745,- Kč.

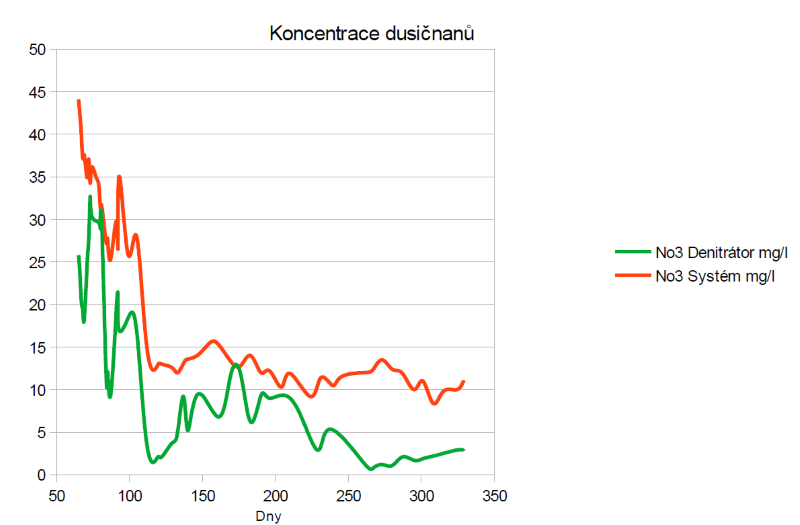
Překvapilo mě, jak citlivě reagoval výstup z denitrátoru na jakoukoliv manipulaci s dávkou metanolu. Zdánlivě po malé redukci dávky pro zpomalení reakce se tato takřka zastavila.
Z grafu výše je patrné, že koncentrace dusičnanů na výstupu z denitrátoru kolísá mnohem výrazněji než koncentrace v systému. To mě přivedlo na myšlenku provést dodatečná měření – nejprve jsme měřili denní průběh po hodině a zjistili jsme kolísání takřka 100 % mezi měřeními. Je jasné, že reakce je silně vázána na dávku metanolu, která probíhá jedenkrát za dvě hodiny. Proto jsme změřili jedno dvouhodinové okno po 11 minutách – výsledek vidíte na grafu níže. Nejnižší koncentrace dusičnanů na výstupu je cca 40–50 minut po nadávkování metanolu, to vidíme prudký propad, poté se reakce lineárně zpomaluje až do další dávky.
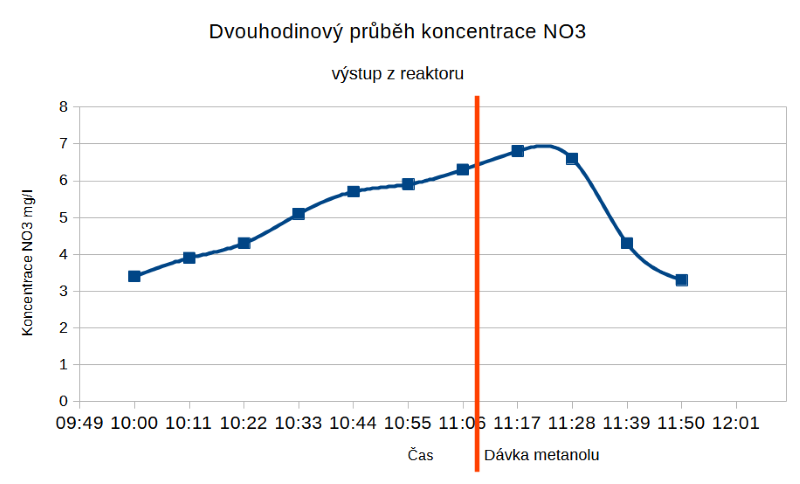
Bylo by výhodné použít menší dávku častěji? Důležité je, že se pohybujeme v bezpečných mezích – dusičnany nikdy neklesnou na nulu ani nevystoupají na stejnou hodnotu, jako má vstupní voda. Dávkovací čerpadlo má určitou přesnost a při poloviční dávce každou hodinu by tato dávka byla natolik nízká, že nepřesnost už by byla značná.
Další příjemné překvapení plyne z běžného provozu reaktoru – za posledních 200 dnů, kdy jsme naposledy upravili dávkování, se drží koncentrace dusičnanů v systému v rozmezí 9,2–15,5 mg/l bez jakýchkoliv zásahů do chodu denitrifikačního filtru.
Za první rok provozu navíc zatím nebylo zapotřebí filtr nijak čistit. Je vidět, že uvnitř reaktoru probíhá pravá denitrifikace, tzn. že dusičnany jsou redukovány metabolismem bakterií a nikoliv nárůstem biomasy.
Zajímavý vedlejší produkt denitrifikace byl pozorovaný prudký nárůst alkality. Ta vystoupala až ke hranici bezpečného rozpětí, za které pokládám 8–12 °dKH (konkrétně nejvyšší naměřená hodnota byla 11,8 °dKH). Z toho důvodu jsme měli připravenou kyselinu chlorovodíkovou, kterou se dá alkalita v mořském akváriu rychle snížit. Nakonec její použití nebylo nutné. Při nitrifikační reakci (oxidaci amoniaku) se alkalita snižuje, při denitrifikaci se stejné množství alkality uvolní zpět. Náš případ byl extrémní – za pár měsíců jsme odstranili akumulaci za více než 10 let. Mořské akvárium, hlavně je-li osázené korály, alkalitu potřebuje a spotřebovává – je tedy třeba pravidelně doplňovat.
A praktické výsledky – dopad na život v akváriích? Hlavním cílem bylo umožnění chovu měkkých i tvrdých korálů. Pokusně jsme osázeli první nádrž a je vidět růst jak jednodušších druhů rodu Capnella nebo Sarcophyton, tak i tvrdých korálů jako Montipora confusa nebo Montipora foliosa. I kondice a vybarvení ryb se pocitově zlepšila a některé druhy se začaly v nádržích třít (Abudefduf vaigiensis, Dascyllus melanurus).
Závěr
Anaerobní denitrifikační filtr je velmi efektivní zařízení pro snižování koncentrace dusičnanů. Při dodržení bezpečnostních zásad je jeho použití zcela bezpečné a nenáročné na obsluhu. Samozřejmě hraje velkou roli škála – čím větší je systém a denitrifikační komora, tím snazší je vyladit procesy, které v ní probíhají, a minimalizovat případná rizika.

(Foto: Mikuláš Velenský)

(Foto: Mikuláš Velenský & Miroslav Buršík)